Atom adalah suatu satuan dasar
materi, yang terdiri atas
inti atom serta awan
elektron bermuatan negatif yang mengelilinginya. Inti atom terdiri atas
proton yang bermuatan positif, dan
neutron yang bermuatan netral (kecuali pada inti atom
Hidrogen-1, yang tidak memiliki neutron). Elektron-elektron pada sebuah atom terikat pada inti atom oleh
gaya elektromagnetik. Sekumpulan atom demikian pula dapat berikatan satu sama lainnya, dan membentuk sebuah
molekul. Atom yang mengandung jumlah proton dan elektron yang sama bersifat netral, sedangkan yang mengandung jumlah proton dan elektron yang berbeda bersifat positif atau negatif dan disebut sebagai
ion. Atom dikelompokkan berdasarkan jumlah proton dan neutron yang terdapat pada inti atom tersebut. Jumlah proton pada atom menentukan
unsur kimia atom tersebut, dan jumlah
neutron menentukan
isotop unsur tersebut.
Istilah atom berasal dari
Bahasa Yunani (ἄτομος/átomos, α-τεμνω), yang berarti tidak dapat dipotong ataupun sesuatu yang tidak dapat dibagi-bagi lagi. Konsep atom sebagai komponen yang tak dapat dibagi-bagi lagi pertama kali diajukan oleh para filsuf
India dan
Yunani. Pada abad ke-17 dan ke-18, para
kimiawan meletakkan dasar-dasar pemikiran ini dengan menunjukkan bahwa zat-zat tertentu tidak dapat dibagi-bagi lebih jauh lagi menggunakan metode-metode kimia. Selama akhir abad ke-19 dan awal abad ke-20, para
fisikawan berhasil menemukan struktur dan komponen-komponen subatom di dalam atom, membuktikan bahwa 'atom' tidaklah tak dapat dibagi-bagi lagi. Prinsip-prinsip
mekanika kuantum yang digunakan para fisikawan kemudian berhasil memodelkan atom.
[1]
Dalam pengamatan sehari-hari, secara relatif atom dianggap sebuah objek yang sangat kecil yang memiliki massa yang secara proporsional kecil pula. Atom hanya dapat dipantau dengan menggunakan peralatan khusus seperti
mikroskop gaya atom. Lebih dari 99,9% massa atom berpusat pada inti atom,
[catatan 1] dengan proton dan neutron yang bermassa hampir sama. Setiap unsur paling tidak memiliki satu isotop dengan inti yang tidak stabil, yang dapat mengalami
peluruhan radioaktif. Hal ini dapat mengakibatkan
transmutasi, yang mengubah jumlah proton dan neutron pada inti.
[2] Elektron yang terikat pada atom mengandung sejumlah
aras energi, ataupun
orbital, yang stabil dan dapat mengalami transisi di antara aras tersebut dengan menyerap ataupun memancarkan
foton yang sesuai dengan perbedaan energi antara aras. Elektron pada atom menentukan sifat-sifat kimiawi sebuah unsur, dan memengaruhi sifat-sifat
magnetis atom tersebut.
Konsep bahwa materi terdiri dari satuan-satuan terpisah yang tidak dapat dibagi lagi menjadi satuan yang lebih kecil telah ada selama satu
milenium. Namun, pemikiran tersebut masihlah bersifat abstrak dan filosofis, daripada berdasarkan pengamatan
empiris dan
eksperimen. Secara filosofis, deskripsi sifat-sifat atom bervariasi tergantung pada budaya dan aliran filosofi tersebut, dan seringkali pula mengandung unsur-unsur spiritual di dalamnya. Walaupun demikian, pemikiran dasar mengenai atom dapat diterima oleh para ilmuwan ribuan tahun kemudian, karena ia secara elegan dapat menjelaskan penemuan-penemuan baru pada bidang kimia.
[3]
Rujukan paling awal mengenai konsep atom dapat ditilik kembali kepada zaman
India kuno pada tahun 800 sebelum masehi,
[4] yang dijelaskan dalam naskah filsafat
Jainisme sebagai
anu dan
paramanu.
[4][5] Aliran mazhab
Nyaya dan
Vaisesika mengembangkan teori yang menjelaskan bagaimana atom-atom bergabung menjadi benda-benda yang lebih kompleks.
[6] Satu abad kemudian muncul rujukan mengenai atom di dunia Barat oleh
Leukippos, yang kemudian oleh muridnya
Demokritos pandangan tersebut disistematiskan. Kira-kira pada tahun 450 SM, Demokritos menciptakan istilah
átomos (
bahasa Yunani:
ἄτομος), yang berarti "tidak dapat dipotong" ataupun "tidak dapat dibagi-bagi lagi". Teori Demokritos mengenai atom bukanlah usaha untuk menjabarkan suatu fenomena fisis secara rinci, melainkan suatu filosofi yang mencoba untuk memberikan jawaban atas perubahan-perubahan yang terjadi pada alam.
[1] Filosofi serupa juga terjadi di India, namun demikian ilmu pengetahuan modern memutuskan untuk menggunakan istilah "atom" yang dicetuskan oleh Demokritos.
[3]
Kemajuan lebih jauh pada pemahaman mengenai atom dimulai dengan berkembangnya ilmu
kimia. Pada tahun 1661,
Robert Boyle mempublikasikan buku
The Sceptical Chymist yang berargumen bahwa materi-materi di dunia ini terdiri dari berbagai kombinasi
"corpuscules", yaitu atom-atom yang berbeda. Hal ini berbeda dengan pandangan klasik yang berpendapat bahwa materi terdiri dari unsur-unsur udara, tanah, api, dan air.
[7] Pada tahun 1789, istilah
element (
unsur) didefinisikan oleh seorang bangsawan dan peneliti Perancis,
Antoine Lavoisier, sebagai bahan dasar yang tidak dapat dibagi-bagi lebih jauh lagi dengan menggunakan metode-metode kimia.
[8]

Berbagai atom dan molekul yang digambarkan pada buku
John Dalton,
A New System of Chemical Philosophy (1808).
Pada tahun 1803,
John Dalton menggunakan konsep atom untuk menjelaskan mengapa unsur-unsur selalu bereaksi dalam perbandingan yang bulat dan tetap, serta mengapa gas-gas tertentu lebih larut dalam air dibandingkan dengan gas-gas lainnya. Ia mengajukan pendapat bahwa setiap unsur mengandung atom-atom tunggal unik, dan atom-atom tersebut selanjutnya dapat bergabung untuk membentuk senyawa-senyawa kimia.
[9][10]
Teori partikel ini kemudian dikonfirmasikan lebih jauh lagi pada tahun 1827, yaitu ketika
botaniwan Robert Brown menggunakan
mikroskop untuk mengamati debu-debu yang mengambang di atas air dan menemukan bahwa debu-debu tersebut bergerak secara acak. Fenomena ini kemudian dikenal sebagai "
Gerak Brown". Pada tahun 1877, J. Desaulx mengajukan pendapat bahwa fenomena ini disebabkan oleh gerak termal molekul air, dan pada tahun 1905
Albert Einstein membuat analisis matematika terhadap gerak ini.
[11][12][13] Fisikawan Perancis
Jean Perrin kemudian menggunakan hasil kerja Einstein untuk menentukan massa dan dimensi atom secara eksperimen, yang kemudian dengan pasti menjadi verifikasi atas teori atom Dalton.
[14]
Berdasarkan hasil penelitiannya terhadap
sinar katoda, pada tahun 1897
J. J. Thomson menemukan elektron dan sifat-sifat subatomiknya. Hal ini meruntuhkan konsep atom sebagai satuan yang tidak dapat dibagi-bagi lagi.
[15] Thomson percaya bahwa elektron-elektron terdistribusi secara merata di seluruh atom, dan muatan-muatannya diseimbangkan oleh keberadaan lautan muatan positif (
model puding prem).
Namun pada tahun 1909, para peneliti di bawah arahan
Ernest Rutherford menembakkan ion helium ke lembaran tipis emas, dan menemukan bahwa sebagian kecil ion tersebut dipantulkan dengan sudut pantulan yang lebih tajam dari yang apa yang diprediksikan oleh teori Thomson. Rutherford kemudian mengajukan pendapat bahwa muatan positif suatu atom dan kebanyakan massanya terkonsentrasi pada inti atom, dengan elektron yang mengitari inti atom seperti planet mengitari matahari. Muatan positif ion helium yang melewati inti padat ini haruslah dipantulkan dengan sudut pantulan yang lebih tajam. Pada tahun 1913, ketika bereksperimen dengan hasil proses
peluruhan radioaktif,
Frederick Soddy menemukan bahwa terdapat lebih dari satu jenis atom pada setiap posisi tabel periodik.
[16] Istilah
isotop kemudian diciptakan oleh
Margaret Todd sebagai nama yang tepat untuk atom-atom yang berbeda namun merupakan satu unsur yang sama. J.J. Thomson selanjutnya menemukan teknik untuk memisahkan jenis-jenis atom tersebut melalui hasil kerjanya pada gas yang terionisasi.
[17]
Sementara itu, pada tahun 1913 fisikawan
Niels Bohr mengkaji ulang model atom Rutherford dan mengajukan pendapat bahwa elektron-elektron terletak pada orbit-orbit yang terkuantisasi serta dapat meloncat dari satu orbit ke orbit lainnya, meskipun demikian tidak dapat dengan bebas berputar spiral ke dalam maupun keluar dalam keadaan transisi.
[18] Suatu elektron haruslah menyerap ataupun memancarkan sejumlah energi tertentu untuk dapat melakukan transisi antara orbit-orbit yang tetap ini. Apabila
cahaya dari materi yang dipanaskan memancar melalui prisma, ia menghasilkan suatu
spektrum multiwarna. Penampakan garis-garis spektrum tertentu ini berhasil dijelaskan oleh teori transisi orbital ini.
[19]
Ikatan kimia antar atom kemudian pada tahun 1916 dijelaskan oleh
Gilbert Newton Lewis sebagai interaksi antara elektron-elektron atom tersebut.
[20] Atas adanya keteraturan sifat-sifat kimiawi dalam tabel periode kimia,
[21] kimiawan Amerika
Irving Langmuir tahun 1919 berpendapat bahwa hal ini dapat dijelaskan apabila elektron-elektron pada sebuah atom saling berhubungan atau berkumpul dalam bentuk-bentuk tertentu. Sekelompok elektron diperkirakan menduduki satu set
kelopak elektron di sekitar inti atom.
Percobaan Stern-Gerlach pada tahun 1922 memberikan bukti lebih jauh mengenai sifat-sifat kuantum atom. Ketika seberkas atom perak ditembakkan melalui medan magnet, berkas tersebut terpisah-pisah sesuai dengan arah momentum sudut atom (
spin). Oleh karena arah spin adalah acak, berkas ini diharapkan menyebar menjadi satu garis. Namun pada kenyataannya berkas ini terbagi menjadi dua bagian, tergantung dari apakah spin atom tersebut berorientasi ke atas ataupun ke bawah.
[22]
Pada tahun 1926, dengan menggunakan pemikiran
Louis de Broglie bahwa partikel berperilaku seperti gelombang, Erwin Schrödinger mengembangkan suatu model atom matematis yang menggambarkan elektron sebagai
gelombang tiga dimensi daripada sebagai titik-titik partikel. Konsekuensi penggunaan bentuk gelombang untuk menjelaskan elektron ini adalah bahwa adalah tidak mungkin untuk secara matematis menghitung
posisi dan
momentum partikel secara bersamaan. Hal ini kemudian dikenal sebagai
prinsip ketidakpastian, yang dirumuskan oleh
Werner Heisenberg pada 1926. Menurut konsep ini, untuk setiap pengukuran suatu posisi, seseorang hanya bisa mendapatkan kisaran nilai-nilai probabilitas momentum, demikian pula sebaliknya. Walaupun model ini sulit untuk divisualisasikan, ia dapat dengan baik menjelaskan sifat-sifat atom yang terpantau yang sebelumnya tidak dapat dijelaskan oleh teori mana pun. Oleh sebab itu, model atom yang menggambarkan elektron mengitari inti atom seperti planet mengitari matahari digugurkan dan digantikan oleh model
orbital atom di sekitar inti di mana elektron paling berkemungkinan berada.
[23][24]

Diagram skema spetrometer massa sederhana.
Perkembangan pada
spektrometri massa mengijinkan dilakukannya pengukuran massa atom secara tepat. Peralatan spektrometer ini menggunakan magnet untuk membelokkan trayektori berkas ion, dan banyaknya defleksi ditentukan dengan rasio massa atom terhadap muatannya. Kimiawan
Francis William Aston menggunakan peralatan ini untuk menunjukkan bahwa isotop mempunyai massa yang berbeda. Perbedaan massa antar isotop ini berupa bilangan bulat, dan ia disebut sebagai
kaidah bilangan bulat.
[25] Penjelasan pada perbedaan massa isotop ini berhasil dipecahkan setelah ditemukannya
neutron, suatu partikel bermuatan netral dengan massa yang hampir sama dengan
proton, yaitu oleh
James Chadwick pada tahun 1932. Isotop kemudian dijelaskan sebagai unsur dengan jumlah proton yang sama, namun memiliki jumlah neutron yang berbeda dalam inti atom.
[26]
Pada tahun 1950-an, perkembangan
pemercepat partikel dan
detektor partikel mengijinkan para ilmuwan mempelajari dampak-dampak dari atom yang bergerak dengan energi yang tinggi.
[27] Neutron dan proton kemudian diketahui sebagai
hadron, yaitu komposit partikel-partikel kecil yang disebut sebagai
kuark. Model-model standar fisika nuklir kemudian dikembangkan untuk menjelaskan sifat-sifat inti atom dalam hal interaksi partikel subatom ini.
[28]
Sekitar tahun 1985,
Steven Chu dkk. di
Bell Labs mengembangkan sebuah teknik untuk menurunkan temperatur atom menggunakan
laser. Pada tahun yang sama, sekelompok ilmuwan yang diketuai oleh
William D. Phillips berhasil memerangkap atom natrium dalam
perangkap magnet.
Claude Cohen-Tannoudji kemudian menggabungkan kedua teknik tersebut untuk mendinginkan sejumlah kecil atom sampai beberapa
mikrokelvin. Hal ini mengijinkan ilmuwan mempelajari atom dengan presisi yang sangat tinggi, yang pada akhirnya membawa para ilmuwan menemukan
kondensasi Bose-Einstein.
[29]
Dalam sejarahnya, sebuah atom tunggal sangatlah kecil untuk digunakan dalam aplikasi ilmiah. Namun baru-baru ini, berbagai peranti yang menggunakan sebuah atom tunggal logam yang dihubungkan dengan
ligan-ligan organik (
transistor elektron tunggal) telah dibuat.
[30] Berbagai penelitian telah dilakukan untuk memerangkap dan memperlambat laju atom menggunakan
pendinginan laser untuk mendapatkan pemahaman yang lebih baik mengenai sifat-sifat atom.
[31]
[sunting] Komponen-komponen atom
[sunting] Partikel subatom
Walaupun awalnya kata
atom berarti suatu partikel yang tidak dapat dipotong-potong lagi menjadi partikel yang lebih kecil, dalam terminologi ilmu pengetahuan modern, atom tersusun atas berbagai
partikel subatom. Partikel-partikel penyusun atom ini adalah
elektron,
proton, dan
neutron. Namun
hidrogen-1 tidak mempunyai neutron. Demikian pula halnya pada
ion hidrogen positif H
+.
Dari kesemua partikel subatom ini, elektron adalah yang paling ringan, dengan massa elektron sebesar 9,11 × 10
−31 kg dan mempunyai muatan negatif. Ukuran elektron sangatlah kecil sedemikiannya tiada teknik pengukuran yang dapat digunakan untuk mengukur ukurannya.
[32] Proton memiliki muatan positif dan massa 1.836 kali lebih berat daripada elektron (1,6726 × 10
−27 kg). Neutron tidak bermuatan listrik dan bermassa bebas 1.839 kali massa elektron
[33] atau (1,6929 × 10
−27 kg).
Dalam model standar fisika, baik proton dan neutron terdiri dari
partikel elementer yang disebut
kuark. Kuark termasuk kedalam golongan partikel
fermion dan merupakan salah satu dari dua bahan penyusun materi dasar (yang lainnya adalah
lepton). Terdapat enam jenis kuark dan tiap-tiap kuark tersebut memiliki muatan listri fraksional sebesar +2/3 ataupun −1/3. Proton terdiri dari dua
kuark naik dan satu
kuark turun, manakala neutron terdiri dari satu kuark naik dan dua kuark turun. Perbedaan komposisi kuark ini memengaruhi perbedaan massa dan muatan antara dua partikel tersebut. Kuark terikat bersama oleh
gaya nuklir kuat yang diperantarai oleh
gluon. Gluon adalah anggota dari
boson tolok yang merupakan perantara gaya-gaya fisika.
[34][35]

Artikel utama untuk bagian ini adalah:
Inti atom 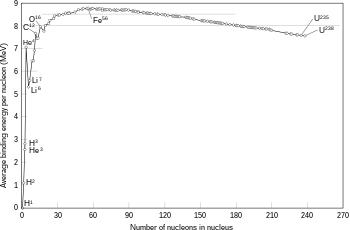
Energi pengikatan yang diperlukan oleh nukleon untuk lolos dari inti pada berbagai isotop.
Inti atom terdiri atas proton dan neutron yang terikat bersama pada pusat atom. Secara kolektif, proton dan neutron tersebut disebut sebagai
nukleon (partikel penyusun inti). Diameter inti atom berkisar antara 10
-15 hingga 10
-14m.
[36] Jari-jari inti diperkirakan sama dengan
![\begin{smallmatrix}1,07 \sqrt[3]{A}\end{smallmatrix}](http://upload.wikimedia.org/wikipedia/id/math/b/5/6/b56e16e37f6036d3414eaf3c1d299f8a.png) fm
fm, dengan
A adalah jumlah nukleon.
[37] Hal ini sangatlah kecil dibandingkan dengan jari-jari atom. Nukleon-nukleon tersebut terikat bersama oleh gaya tarik-menarik potensial yang disebut
gaya kuat residual. Pada jarak lebih kecil daripada 2,5 fm, gaya ini lebih kuat daripada
gaya elektrostatik yang menyebabkan proton saling tolak menolak.
[38]
Atom dari
unsur kimia yang sama memiliki jumlah proton yang sama, disebut
nomor atom. Suatu unsur dapat memiliki jumlah neutron yang bervariasi. Variasi ini disebut sebagai
isotop. Jumlah proton dan neutron suatu atom akan menentukan
nuklida atom tersebut, sedangkan jumlah neutron relatif terhadap jumlah proton akan menentukan stabilitas inti atom, dengan isotop unsur tertentu akan menjalankan
peluruhan radioaktif.
[39]
Neutron dan proton adalah dua jenis
fermion yang berbeda.
Asas pengecualian Pauli melarang adanya keberadaan fermion yang
identik (seperti misalnya proton berganda) menduduki suatu keadaan fisik kuantum yang sama pada waktu yang sama. Oleh karena itu, setiap proton dalam inti atom harusnya menduduki keadaan kuantum yang berbeda dengan aras energinya masing-masing. Asas Pauli ini juga berlaku untuk neutron. Pelarangan ini tidak berlaku bagi proton dan neutron yang menduduki keadaan kuantum yang sama.
[40]
Untuk atom dengan nomor atom yang rendah, inti atom yang memiliki jumlah proton lebih banyak daripada neutron berpotensi jatuh ke keadaan energi yang lebih rendah melalui peluruhan radioaktif yang menyebabkan jumlah proton dan neutron seimbang. Oleh karena itu, atom dengan jumlah proton dan neutron yang berimbang lebih stabil dan cenderung tidak meluruh. Namun, dengan meningkatnya nomor atom, gaya tolak-menolak antar proton membuat inti atom memerlukan proporsi neutron yang lebih tinggi lagi untuk menjaga stabilitasnya. Pada inti yang paling berat, rasio neutron per proton yang diperlukan untuk menjaga stabilitasnya akan meningkat menjadi 1,5.
[40]
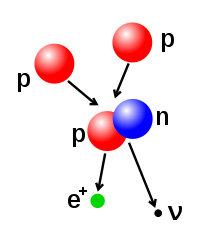
Gambaran proses fusi nuklir yang menghasilkan inti deuterium (terdiri dari satu proton dan satu neutron). Satu
positron (e
+) dipancarkan bersamaan dengan
neutrino elektron.
Jumlah proton dan neutron pada inti atom dapat diubah, walaupun hal ini memerlukan energi yang sangat tinggi oleh karena gaya atraksinya yang kuat.
Fusi nuklir terjadi ketika banyak partikel atom bergabung membentuk inti yang lebih berat. Sebagai contoh, pada inti Matahari, proton memerlukan energi sekitar 3–10 keV untuk mengatasi gaya tolak-menolak antar sesamanya dan bergabung menjadi satu inti.
[41] Fisi nuklir merupakan kebalikan dari proses fusi. Pada fisi nuklir, inti dipecah menjadi dua inti yang lebih kecil. Hal ini biasanya terjadi melalui peluruhan radioaktif. Inti atom juga dapat diubah melalui penembakan partikel subatom berenergi tinggi. Apabila hal ini mengubah jumlah proton dalam inti, atom tersebut akan berubah unsurnya.
[42][43]
Jika massa inti setelah terjadinya reaksi fusi lebih kecil daripada jumlah massa partikel awal penyusunnya, maka perbedaan ini disebabkan oleh pelepasan pancaran energi (misalnya
sinar gamma), sebagaimana yang ditemukan pada rumus
kesetaraan massa-energi Einstein,
E =
mc2, dengan
m adalah massa yang hilang dan
c adalah
kecepatan cahaya. Defisit ini merupakan bagian dari
energi pengikatan inti yang baru.
[44]
Fusi dua inti yang menghasilkan inti yang lebih besar dengan nomor atom lebih rendah daripada
besi dan
nikel (jumlah total nukleon sama dengan 60) biasanya bersifat
eksotermik, yang berarti bahwa proses ini melepaskan energi.
[45] Adalah proses pelepasan energi inilah yang membuat fusi nuklir pada
bintang dapat dipertahankan. Untuk inti yang lebih berat, energi pengikatan per
nukleon dalam inti mulai menurun. Ini berarti bahwa proses fusi akan bersifat
endotermik.
[40]
[sunting] Awan elektron

Sumur potensial yang menunjukkan energi minimum
V(
x) yang diperlukan untuk mencapai tiap-tiap posisi
x. Suatu partikel dengan energi
E dibatasi pada kisaran posisi antara
x1 dan
x2.
Elektron dalam suatu atom ditarik oleh proton dalam inti atom melalui
gaya elektromagnetik. Gaya ini mengikat elektron dalam sumur potensi elektrostatik di sekitar inti. Hal ini berarti bahwa energi luar diperlukan agar elektron dapat lolos dari atom. Semakin dekat suatu elektron dalam inti, semakin besar gaya atraksinya, sehingga elektron yang berada dekat dengan pusat sumur potensi memerlukan energi yang lebih besar untuk lolos.
Elektron, sama seperti partikel lainnya, memiliki sifat seperti partikel maupun seperti gelombang (dualisme gelombang-partikel). Awan elektron adalah suatu daerah dalam sumur potensi di mana tiap-tiap elektron menghasilkan sejenis gelombang diam (yaitu gelombang yang tidak bergerak relatif terhadap inti) tiga dimensi. Perilaku ini ditentukan oleh
orbital atom, yakni suatu fungsi matematika yang menghitung probabilitas suatu elektron akan muncul pada suatu lokasi tertentu ketika posisinya diukur.
[46] Hanya akan ada satu himpunan orbital tertentu yang berada disekitar inti, karena pola-pola gelombang lainnya akan dengan cepat meluruh menjadi bentuk yang lebih stabil.
[47]

Fungsi gelombang dari lima orbital atom pertama. Tiga orbital 2p memperlihatkan satu biidang simpul.
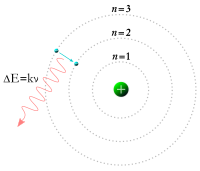
Tiap-tiap orbital atom berkoresponden terhadap
aras energi elektron tertentu. Elektron dapat berubah keadaannya ke aras energi yang lebih tinggi dengan menyerap sebuah
foton. Selain dapat naik menuju aras energi yang lebih tinggi, suatu elektron dapat pula turun ke keadaan energi yang lebih rendah dengan memancarkan energi yang berlebih sebagai foton.
[47]
Energi yang diperlukan untuk melepaskan ataupun menambah satu elektron (energi pengikatan elektron) adalah lebih kecil daripada energi pengikatan nukleon. Sebagai contohnya, hanya diperlukan 13,6 eV untuk melepaskan elektron dari atom hidrogen.
[48] Bandingkan dengan energi sebesar 2,3 MeV yang diperlukan untuk memecah inti
deuterium.
[49] Atom bermuatan listrik netral oleh karena jumlah proton dan elektronnya yang sama. Atom yang kekurangan ataupun kelebihan elektron disebut sebagai
ion. Elektron yang terletak paling luar dari inti dapat ditransfer ataupun dibagi ke atom terdekat lainnya. Dengan cara inilah, atom dapat saling
berikatan membentuk
molekul.
[50]

 Lavoisier mengelompokkan zat-zat yang dipercaya sebagai unsur (seperti cahaya, kalori dan beberapa senyawa) berdasarkan sifat kimianya menjadi gas, non-logam dan tanah.
Lavoisier mengelompokkan zat-zat yang dipercaya sebagai unsur (seperti cahaya, kalori dan beberapa senyawa) berdasarkan sifat kimianya menjadi gas, non-logam dan tanah.

 Dalam daftar massa unsur yang dibuat oleh Dalton terdapat kesalahan dalam penentuan massa atom unsur. Pada tahun 1828 Barzellius berhasil membuat dan mempublikasikan daftar massa atom unsur-unsur yang lebih akurat.
Dalam daftar massa unsur yang dibuat oleh Dalton terdapat kesalahan dalam penentuan massa atom unsur. Pada tahun 1828 Barzellius berhasil membuat dan mempublikasikan daftar massa atom unsur-unsur yang lebih akurat. Pada tahun 1829, Johann Dőbereiner mengklasifikasikan unsur berdasarkan kemiripan sifat-sifatnya yang disebut sebagai triad Dobereiner. Dalam aturan ini, bila unsur-unsur dikelompokkan berdasarkan kesamaan sifat dan massa atomnya kemudian diurutkan, maka setiap kelompok akan terdiri dari tiga unsur dan massa atom unsur yang ditengah adalah rata-rata dari jumlah kedua atom unsur yang di tepi.
Pada tahun 1829, Johann Dőbereiner mengklasifikasikan unsur berdasarkan kemiripan sifat-sifatnya yang disebut sebagai triad Dobereiner. Dalam aturan ini, bila unsur-unsur dikelompokkan berdasarkan kesamaan sifat dan massa atomnya kemudian diurutkan, maka setiap kelompok akan terdiri dari tiga unsur dan massa atom unsur yang ditengah adalah rata-rata dari jumlah kedua atom unsur yang di tepi. 

 Pada tahun 1865, mengelompokkan unsur-unsur berdasarkan kenaikan massa atom. Ia mengamati setiap pengulangan delapan unsur akan terdapat kemiripan sifat. Dengan demikian berarti unsur kesatu mirip unsur kedelapan, unsur kedua mirip unsur kesembilan demikian seterusnya. Newlands menyebut pengulangan ini sebagai hukum oktaf.
Pada tahun 1865, mengelompokkan unsur-unsur berdasarkan kenaikan massa atom. Ia mengamati setiap pengulangan delapan unsur akan terdapat kemiripan sifat. Dengan demikian berarti unsur kesatu mirip unsur kedelapan, unsur kedua mirip unsur kesembilan demikian seterusnya. Newlands menyebut pengulangan ini sebagai hukum oktaf.



 Pada tahun 1869 Mendeleev membuat sistem periodik berdasarkan kenaikan massa atom dan kemiripan sifat. Unsur-unsur dengan sifat yang mirip ditempatkan pada kolom yang disebut golongan. Sedangkan pengulangan sifat menghasilkan baris yang disebut periode.
Pada tahun 1869 Mendeleev membuat sistem periodik berdasarkan kenaikan massa atom dan kemiripan sifat. Unsur-unsur dengan sifat yang mirip ditempatkan pada kolom yang disebut golongan. Sedangkan pengulangan sifat menghasilkan baris yang disebut periode.







![\begin{smallmatrix}1,07 \sqrt[3]{A}\end{smallmatrix}](http://upload.wikimedia.org/wikipedia/id/math/b/5/6/b56e16e37f6036d3414eaf3c1d299f8a.png)






